患者父亲代签知情同意书,患者本人起诉医院赔偿166万
发布日期:2022-04-25 作者:张勇律师
作者:医法汇
转载请注明来源:医法汇
案情简介
患者吴先生(26岁),10年前父母离婚,法院判决其由父亲吴某抚养。因患者情绪不稳定,怀疑自己被害以及冲动打人加重2个月,被其父亲送到市精神医院住院治疗,被诊断为未分化型精神分裂症,其父亲作为监护人在《非自愿住院治疗知情同意书》签名。
住院期间,医院告知患者及其父亲有关药品临床试验的内容、风险及获益,患者及其父亲阅读知情同意书后,自愿参加临床试验并签署了《临床试验知情同意书》,受试者签名处有患者本人字迹,法定监护人签名处有其父亲吴某字迹,与受试者关系处有手写“父子”字迹。之后,医院进行随机、双盲双模拟、阳性药平行对照临床研究。一个月后,患者家属要求出院,医院认为患者病情欠稳定不适宜出院,患者家属自愿承担复发风险,经上级医师同意,予以出院。患者出院后经常处于精神分裂状态,于起诉前1年取得残疾人证(二级),证上的联系人为其父亲吴某。
患者认为,其系非自愿入院,医院在给其做临床药物试验时,并未严格按照药物的临床试验技术指导原则,检测其是否符合该项药物临床试验,且知情同意书上也未经其本人签字确认,侵犯了知情同意权,并造成了残疾的损害后果,由其母亲作为诉讼代理人,起诉医院赔偿医药费、误工费、残疾赔偿金等损失共计166万余元。
法院审理
诉讼中,法院追加患者父亲吴某作为第三人参加诉讼。经笔迹鉴定,《临床试验知情同意书》受试者签名“吴先生”字迹与提供的“吴先生”样本字迹不是同一人书写。法定监护人签名处“吴某”字迹与提供的样本字迹是同一人书写。
法院另查明,本次药物临床试验经过了伦理委员会审批,并向相关部门备案。
一审法院认为,患者属于非自愿入院收治情形,且其父亲作为监护人在《临床试验知情同意书》上进行了签字确认,应认定患者参加试验已经取得其监护人的同意,故不构成侵害患者的知情同意权。患者没有提供充分证据证明其因接受临床试验造成损害后果以及存在因果关系,判决驳回全部诉讼请求。
患者不服判决提起上诉,二审法院判决驳回上诉,维持原判。

法律简析
药物临床试验研究是推动医学发展和提高医疗水平的不竭动力。在临床试验中,受试者可能遭受的医疗损害以及知情同意是此类医疗纠纷案件的争议焦点。
受试者知情同意权,是本案的核心问题。伦理审查与知情同意是保障受试者权益的重要措施。这里的知情同意,是指受试者被告知可影响其做出参加临床试验决定的各方面情况后,确认同意自愿参加临床试验的过程。该过程应当以书面的、签署姓名和日期的知情同意书作为文件证明。受试者或者其监护人,以及执行知情同意的研究者应当在知情同意书上分别签名并注明日期,如非受试者本人签署,应当注明关系。受试者为无民事行为能力的,应当取得其监护人的书面知情同意;受试者为限制民事行为能力的,应当取得本人及其监护人的书面知情同意。当监护人代表受试者知情同意时,应当在受试者可理解的范围内告知受试者临床试验的相关信息,并尽量让受试者亲自签署知情同意书和注明日期。
同时,医疗机构对精神障碍患者实施与精神障碍治疗有关的实验性临床医疗时,应当向患者或者其监护人告知医疗风险、替代医疗方案等情况,并取得患者的书面同意;无法取得患者意见的,应当取得其监护人的书面同意,并经本医疗机构伦理委员会批准。
由此可知,药物临床试验知情告知对象的第一顺位应当是具有完全民事行为能力的患者本人,其次是患者的法定代理人。本案中,患者经诊断为精神障碍患者,且非自愿住院治疗,此情形下,市医院取得其监护人的书面同意并无不当。经鉴定《临床试验知情同意书》法定监护人签名处有其父亲吴某的签名,因此法院认定市医院并未侵犯患者的知情同意权。
据国家药监局药品审评中心于2021 年 11 月发布的《中国新药注册临床试验现状年度报告(2020年)》数据显示,2020年度共登记临床试验2602项,较2019年总体增长9.1%(2386项)。按新药(即非生物等效性临床试验品种)和仿制药类别(含仿制药质量和疗效一致性评价)统计临床试验登记量,新药高于仿制药,占比分别为57%(1473项)和43%(1129项)。
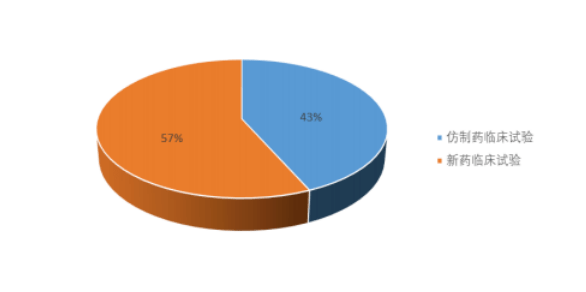
(图片来源:国家药监局药品审评中心)
药物临床试验可以随机分配,亦称随机分组,包括简单随机、区组随机、分层随机及适应性随机等,设盲方式包括双盲、单盲或非盲。参与临床试验的每位受试者的分组过程必须满足以下两点:一方面是不可预测性,指受试者、研究者以及参与试验的其他相关人员,均不应在随机分配实施前预先知晓或预测到治疗分配的相关信息。另一方面是机会均等,指在一定条件下(例如,在分层随机中的一定条件是指同一层内),每位受试者被分配到同一治疗组的概率相等。同时注意,随机分配到不同治疗组的概率可以相等(平衡设计),也可以不等(非平衡设计)。本案中,患者所参与的临床试验即为双盲方式,而在揭盲之后患者服用的并非试验用药,其认为系试验用药导致了损害后果发生,显然是没有依据的,依据“谁主张,谁举证”的原则,患方因未完成举证责任,故而未获法院支持。
我们也应该注意到,无论是常规诊疗活动还是开展临床试验,医疗机构在选择告知对象时既要尊重患者的意愿,也要符合相关法律的要求,应以取得患者本人知情同意为原则,以取得近亲属或法定监护人知情同意为补充,同时要保留好相关证据,从而规避未尽告知义务而承担责任的法律风险。
(本文系医法汇原创,根据真实案例改编,为保护当事人隐私均采用化名)
转载请注明来源:医法汇
案情简介
患者吴先生(26岁),10年前父母离婚,法院判决其由父亲吴某抚养。因患者情绪不稳定,怀疑自己被害以及冲动打人加重2个月,被其父亲送到市精神医院住院治疗,被诊断为未分化型精神分裂症,其父亲作为监护人在《非自愿住院治疗知情同意书》签名。
住院期间,医院告知患者及其父亲有关药品临床试验的内容、风险及获益,患者及其父亲阅读知情同意书后,自愿参加临床试验并签署了《临床试验知情同意书》,受试者签名处有患者本人字迹,法定监护人签名处有其父亲吴某字迹,与受试者关系处有手写“父子”字迹。之后,医院进行随机、双盲双模拟、阳性药平行对照临床研究。一个月后,患者家属要求出院,医院认为患者病情欠稳定不适宜出院,患者家属自愿承担复发风险,经上级医师同意,予以出院。患者出院后经常处于精神分裂状态,于起诉前1年取得残疾人证(二级),证上的联系人为其父亲吴某。
患者认为,其系非自愿入院,医院在给其做临床药物试验时,并未严格按照药物的临床试验技术指导原则,检测其是否符合该项药物临床试验,且知情同意书上也未经其本人签字确认,侵犯了知情同意权,并造成了残疾的损害后果,由其母亲作为诉讼代理人,起诉医院赔偿医药费、误工费、残疾赔偿金等损失共计166万余元。
法院审理
诉讼中,法院追加患者父亲吴某作为第三人参加诉讼。经笔迹鉴定,《临床试验知情同意书》受试者签名“吴先生”字迹与提供的“吴先生”样本字迹不是同一人书写。法定监护人签名处“吴某”字迹与提供的样本字迹是同一人书写。
法院另查明,本次药物临床试验经过了伦理委员会审批,并向相关部门备案。
一审法院认为,患者属于非自愿入院收治情形,且其父亲作为监护人在《临床试验知情同意书》上进行了签字确认,应认定患者参加试验已经取得其监护人的同意,故不构成侵害患者的知情同意权。患者没有提供充分证据证明其因接受临床试验造成损害后果以及存在因果关系,判决驳回全部诉讼请求。
患者不服判决提起上诉,二审法院判决驳回上诉,维持原判。

法律简析
药物临床试验研究是推动医学发展和提高医疗水平的不竭动力。在临床试验中,受试者可能遭受的医疗损害以及知情同意是此类医疗纠纷案件的争议焦点。
受试者知情同意权,是本案的核心问题。伦理审查与知情同意是保障受试者权益的重要措施。这里的知情同意,是指受试者被告知可影响其做出参加临床试验决定的各方面情况后,确认同意自愿参加临床试验的过程。该过程应当以书面的、签署姓名和日期的知情同意书作为文件证明。受试者或者其监护人,以及执行知情同意的研究者应当在知情同意书上分别签名并注明日期,如非受试者本人签署,应当注明关系。受试者为无民事行为能力的,应当取得其监护人的书面知情同意;受试者为限制民事行为能力的,应当取得本人及其监护人的书面知情同意。当监护人代表受试者知情同意时,应当在受试者可理解的范围内告知受试者临床试验的相关信息,并尽量让受试者亲自签署知情同意书和注明日期。
同时,医疗机构对精神障碍患者实施与精神障碍治疗有关的实验性临床医疗时,应当向患者或者其监护人告知医疗风险、替代医疗方案等情况,并取得患者的书面同意;无法取得患者意见的,应当取得其监护人的书面同意,并经本医疗机构伦理委员会批准。
由此可知,药物临床试验知情告知对象的第一顺位应当是具有完全民事行为能力的患者本人,其次是患者的法定代理人。本案中,患者经诊断为精神障碍患者,且非自愿住院治疗,此情形下,市医院取得其监护人的书面同意并无不当。经鉴定《临床试验知情同意书》法定监护人签名处有其父亲吴某的签名,因此法院认定市医院并未侵犯患者的知情同意权。
据国家药监局药品审评中心于2021 年 11 月发布的《中国新药注册临床试验现状年度报告(2020年)》数据显示,2020年度共登记临床试验2602项,较2019年总体增长9.1%(2386项)。按新药(即非生物等效性临床试验品种)和仿制药类别(含仿制药质量和疗效一致性评价)统计临床试验登记量,新药高于仿制药,占比分别为57%(1473项)和43%(1129项)。

(图片来源:国家药监局药品审评中心)
药物临床试验可以随机分配,亦称随机分组,包括简单随机、区组随机、分层随机及适应性随机等,设盲方式包括双盲、单盲或非盲。参与临床试验的每位受试者的分组过程必须满足以下两点:一方面是不可预测性,指受试者、研究者以及参与试验的其他相关人员,均不应在随机分配实施前预先知晓或预测到治疗分配的相关信息。另一方面是机会均等,指在一定条件下(例如,在分层随机中的一定条件是指同一层内),每位受试者被分配到同一治疗组的概率相等。同时注意,随机分配到不同治疗组的概率可以相等(平衡设计),也可以不等(非平衡设计)。本案中,患者所参与的临床试验即为双盲方式,而在揭盲之后患者服用的并非试验用药,其认为系试验用药导致了损害后果发生,显然是没有依据的,依据“谁主张,谁举证”的原则,患方因未完成举证责任,故而未获法院支持。
我们也应该注意到,无论是常规诊疗活动还是开展临床试验,医疗机构在选择告知对象时既要尊重患者的意愿,也要符合相关法律的要求,应以取得患者本人知情同意为原则,以取得近亲属或法定监护人知情同意为补充,同时要保留好相关证据,从而规避未尽告知义务而承担责任的法律风险。
(本文系医法汇原创,根据真实案例改编,为保护当事人隐私均采用化名)
相关法律知识


